[PHV-FC]: Cho hỗn hợp gồm Zn, Al phản ứng vừa đủ với dung dịch gồm HCl và 0,015 mol KNO3. Sau khi kết thúc các phản ứng thu được dung dịch X chứa 8,11 gam muối và 0,896 lít (đktc) hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu trong không khí. Biết rằng tỉ khối của Y so với H2 là 4,50. Khối lượng Al đã tham gia phản ứng là
-
-
-
-
Đáp án đúng: D
HD: Y gồm 0,03 mol H2 và 0,01 mol NO. Để có H2 → phải hết NO3– trong dung dịch đã.
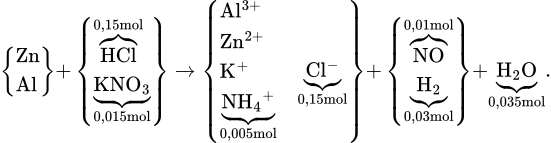
Ở trên; nH2O = 2nNO + 3nNH4+ = 0,035 mol theo ghép cụm ||→ có 0,15 mol HCl theo bảo toàn H.
||→ Gọi số mol Zn, Al tương ứng là x và y mol thì có:
2x + 3y = 0,15 – 0,005 – 0,015 (theo bảo toàn điện tích trong X).
Lại có: mmuối trong X = 65x + 27y + 0,015 × 39 + 0,005 × 18 + 0,15 × 35,5 = 81,1 gam.
Giải hệ được x = 0,02 mol và y = 0,03 mol. ||→ mAl phản ứng = 0,810 gam. Chọn đáp án D. ♠.
► Hướng khác, tiếp cận theo cách viết sơ đồ cũ và hướng khác.!
Sơ đồ: 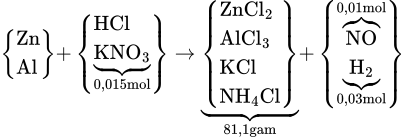
Kiểu sơ đồ này chỉ mang tính chất nhìn quá trình thôi.! phép tính thường đã mặc định + quen:
Bảo toàn electron có: 2x + 3y = 0,01 × 3 + 0,03 × 2 + 0,005 × 8
mmuối = 136x + 133,5y + 0,015 × 74,5 + 0,005 × 80 = 81,1 gam.
Giải hệ được kết quả tương tự như trên thôi.!
Số bình luận về đáp án: 17

Ở trên; nH2O = 2nNO + 3nNH4+ = 0,035 mol theo ghép cụm ||→ có 0,15 mol HCl theo bảo toàn H.
||→ Gọi số mol Zn, Al tương ứng là x và y mol thì có:
2x + 3y = 0,15 – 0,005 – 0,015 (theo bảo toàn điện tích trong X).
Lại có: mmuối trong X = 65x + 27y + 0,015 × 39 + 0,005 × 18 + 0,15 × 35,5 = 81,1 gam.
Giải hệ được x = 0,02 mol và y = 0,03 mol. ||→ mAl phản ứng = 0,810 gam. Chọn đáp án D. ♠.
► Hướng khác, tiếp cận theo cách viết sơ đồ cũ và hướng khác.!
Sơ đồ:

Kiểu sơ đồ này chỉ mang tính chất nhìn quá trình thôi.! phép tính thường đã mặc định + quen:
Bảo toàn electron có: 2x + 3y = 0,01 × 3 + 0,03 × 2 + 0,005 × 8
mmuối = 136x + 133,5y + 0,015 × 74,5 + 0,005 × 80 = 81,1 gam.
Giải hệ được kết quả tương tự như trên thôi.!